Известно, что для возникновения горения необходимо наличие:
1. Горючего вещества
2. Окислителя
3. Источника зажигания (энергетический импульс)
Эти три составляющие часто называют треугольником пожара. Если исключить одну из них, то горение возникнуть не может. Это важнейшее свойство треугольника используется на практике для предотвращения и тушения пожаров.
Воздух и горючее вещество составляют систему, способную гореть, а температурные условия обуславливают возможность самовоспламенения и горения системы.
Наибольшая скорость горения получается при горении вещества в чистом кислороде, наименьшая (прекращение горения) – при содержании 14–15% кислорода.
Горение веществ может происходить за счет кислорода, находящегося в составе других веществ, способных легко его отдавать. Такие вещества называются окислителями. Приведем наиболее известные окислители.
· Бертолетова соль (KClO 3).
· Калийная селитра (KNO 3).
· Натриевая селитра (NaNO 3).
В составе окислителей содержится кислород, который может быть выделен путем разложения соли, например:
2 KClO 3 = 2KCl + 3 O 2
Разложение окислителей происходит при нагревании, а некоторых из них даже под воздействием сильного удара.
2. Продукты горения. Полное и неполное сгорание. Экологические аспекты процессов горения.
В процессе горения образуются продукты сгорания. Состав usшвисит от горящего вещества и условий горения. Продукты сгорания, за исключением окиси углерода, гореть не способны.
Дым, образующийся при горении органических веществ, содержит твердые частицы и газообразные продукты (углекислый газ, окись углерода, азот, сернистый газ и другие). В зависимости от состава веществ и условий их горения получается различный по содержанию дым. Дымы, образующиеся при горении разных веществ, отличаются не только составом, но цветом и запахом. По цвету дыма можно определить, какое вещество горит, хотя цвет дыма изменяется в зависимости от условий трения. При горении древесины дым имеет серовато-черный пнет; бумаги, сена, соломы - беловато-желтый; ткани и хлопка- бурый; нефтепродуктов - черный и т. д.
Продукты горения – это газообразные, жидкие или твердые вещества, образующиеся в процессе горения. Состав продуктов сгорания зависит от состава горящего вещества и от условий его горения. Органические и неорганические горючие вещества состоят, главным образом, из углерода, кислорода, водорода, серы, фосфора и азота. Из них углерод, водород, сера и фосфор способны окисляться при температуре горения и образовывать продукты горения: СО, CO 2 , SO 2 , P 2 O 5 . Азот при температуре горения не окисляется и выделяется в свободном состоянии, а кислород расходуется на окисление горючих элементов вещества. Все указанные продукты сгорания (за исключение окиси углерода СО) гореть в дальнейшем больше не способны. Они образуются при полном сгорании, то есть при горении, которое протекает при доступе достаточного количества воздуха и при высокой температуре.
Углекислый газ или двуокись углерода (СО 2) – продукт полного горения углерода. Не имеет запаха и цвета. Горение магния, например, происходит в атмосфере углекислого газа по уравнению:
CO 2 +2 Mg = C + 2 MgO.
При концентрации углекислого газа в воздухе, превышающей 3-4.5%, нахождение в помещении и вдыхание газа в течение получаса опасно для жизни.
Оксид углерода или угарный газ (СО) – продукт неполного сгорания углерода. Этот газ не имеет запаха и цвета, поэтому особо опасен.
Сернистый газ (SO 2) – продукт горения серы и сернистых соединений. Бесцветный газ с характерным резким запахом.
Дым При горении многих веществ, кроме рассмотренных выше продуктов сгорания выделяется дым – дисперсная система, состоящая из мельчайших твердых частиц, находящихся во взвешенном состоянии в каком-либо газе.
При неполном сгорании органических веществ в условиях низких температур и недостатка воздуха образуются более разнообразные продукты – окись углерода, спирты, кетоны, альдегиды, кислоты и другие сложные химические соединения. Они получаются при частичном окислении как самого горючего, так и продуктов его сухой перегонки (пиролиза). Эти продукты образуют едкий и ядовитый дым. Кроме того, продукты неполного горения сами способны гореть и образовывать с воздухом взрывчатые смеси. Такие взрывы бывают при тушении пожаров в подвалах, сушилках и в закрытых помещениях с большим количеством горючего материала. Рассмотрим кратко свойства основных продуктов горения.
Экологические аспекты процессов горения. Применение природного газа позволяет уменьшить загрязнение атмосферы оксидам серы, твердыми частицами и окисью углерода, однако в атмосферу поступает большое количество оксидов азота, окиси углерода и канцерогенных веществ (3,4-бенз(о)перен). Правильная организация горения, выбор рациональных способов сжигания позволяет свести к минимуму образование вредных веществ и выделение их в воздушный бассейн. Использование природного газа позволяет вести не только пассивную, но и активную борьбу за чистоту воздуха: использование установок для дожигания, использование выбросных газов для подачи в газовый горелки вместо соответствующего количества воздуха.
Экологические проблемы горения. Задача – не навредить при сжигании топлив. Негативные проявления:
Техногенное тепловыделение соизмеримо с компонентами теплового баланса атмосферы;
Акустический шум турбулентных пламен при работе авиационных и ракетных двигателей – загрязнитель окружающей среды.
Выброс вредных продуктов сгорания – окислов азота, окислов металлов, угарного газа (при высоких Тг), окислов серы, канцерогенных веществ – продуктов неполного пиролиза органических горючих, сажи, углекислого газа (при низких Тг) – является причиной: изменения оптических свойств атмосферы и уменьшения потока солнечного излучения, возникновения кислотных дождей, усиления «парникового эффекта», разрушения озонового слоя Земли, негативного воздействия на флору и фауну, здания и конструкции. Общий итог: глобальное потепление, климатические катастрофы (циклоны, бураны, смерчи, цунами, наводнения, засухи, сходы лавин, сели)..
3. Уравнения горения веществ в кислороде и на воздухе, методика их составления. Термодинамика процессов горения. Тепловые эффекты реакций горения.
Общее уравнение реакции горения любого углеводорода
C m H n + (m + n/4) O 2 = mCO 2 + (n/2) Н 2 O + Q (8.1)
где m, n - число атомов углерода и водорода в молекуле; Q - тепловой эффект реакции, или теплота сгорания.
Тепловой эффект (теплота сгорания) Q - количество теплоты, выделяющееся при полном сгорании 1 кмоля, 1 кг или 1 м 3 газа при нормальных физических условиях. Различают высшую Q в и низшую Q н теплоту сгорания: высшая теплота сгорания включает в себя теплоту конденсации водяных паров в процессе горения (в реальности при сжигании газа водяные пары не конденсируются, а удаляются вместе с другими продуктами сгорания). Обычно технические расчеты обычно ведут по низшей теплоте сгорания, без учета теплоты конденсации водяных паров (около 2400 кДж/кг).
КПД, рассчитанный по низшей теплоте сгорания, формально выше, но теплота конденсации водяных паров достаточно велика, и ее использование более чем целесообразно. Подтверждение этому - активное применение в отопительной технике контактных теплообменников, весьма разнообразных по конструкции.
Для смеси горючих газов высшая (и низшая) теплота сгорания газов определяется по соотношению
Q = r 1 Q 1 + r 2 Q 2 + ... + r n Q n (8.2)
где r 1 , r 2 , …, r n - объемные (молярные, массовые) доли компонентов, входящих в смесь; Q 1 , Q 2 , …, Q n - теплота сгорания компонентов.
Процесс горения протекает гораздо сложнее, чем по формуле (8.1), так как наряду с разветвлением цепей происходит их обрыв за счет образования промежуточных стабильных соединений, которые при высокой температуре претерпевают дальнейшие преобразования. При достаточной концентрации кислорода образуются конечные продукты: водяной пар Н 2 О и двуокись углерода СО 2 . При недостатке окислителя, а также при охлаждении зоны реакции, промежуточные соединения могут стабилизироваться и попадать в окружающую среду.
Высокотемпературное горение углеводородов имеет весьма сложный характер и связано с образованием активных частиц в виде атомов и радикалов, а также промежуточных молекулярных соединений. В качестве примера приводятся реакции горения простейшего углеводорода - метана:
1.
Н + О 2 -› ОН + О
СН 4 + ОН -› СН 3 + Н 2 О
СН 4 + О -› СН 2 + Н 2 О
2.
СН 3 + О 2 -› НСНО + ОН
СН 2 + О 2 -› НСНО + О
3.
НСНО + ОН -› НСО + Н 2 О
НСНО + О -› СО + Н 2 О
НСО + О 2 -› СО + О + ОН
4.
СО + О -› СО 2
СО + ОН -› СО 2 + Н
Итог единичного цикла:
2СН 4 + 4О 2 -› 2СО 2 + 4Н 2 О
Термодинамика горения
Исходный состав горючей смеси характеризуется молярными или массовыми долями компонентов и начальными давлением и температурой. Если состав смеси подобран так, что при её сгорании и горючее, и окислитель полностью преобразуются в продукты реакции, то такая смесь называется стехиометрической. Смеси с избытком топлива называются богатыми , а с недостатком топлива - бедными . Степень отклонения состава смеси от стехиометрического характеризуется коэффициентом избытка топлива (англ. equivalenceratio ) :
где Y F и Y O - массовые доли топлива и окислителя соответственно, а (Y F /Y O) st - их отношение в стехиометрической смеси. В русскоязычной литературе используется также коэффициент избытка окислителя (или воздуха), обратный коэффициенту избытка топлива.

Адиабатическая температура горения смесей CH 4 с воздухом в зависимости от коэффициента избытка топлива. P = 1 бар, T 0 = 298,15 K.
Если горение происходит адиабатически при постоянном объёме, то сохраняется полная внутренняя энергия системы, если же при постоянном давлении - то энтальпия системы. На практике условия адиабатического горения приближённо реализуются в свободно распространяющемся пламени (без учёта теплопотерь излучением) и в других случаях, когда потерями тепла из зоны реакции можно пренебречь, например, в камерах сгорания мощных газотурбинных установок или ракетных двигателей.
Адиабатическая температура горения - это температура продуктов, достигаемая при полном протекании химических реакций и установлении термодинамического равновесия. Для термодинамических расчётов используются таблицы термодинамических функций всех компонентов исходной смеси и продуктов. Методы химической термодинамики позволяют рассчитать состав продуктов, конечное давление и температуру при заданных условиях сгорания. В настоящее время доступно много программ, способных выполнять эти расчёты .
Теплота сгорания - это количество теплоты, выделившейся при полном сгорании исходных компонентов, то есть до CO 2 и H 2 O для углеводородных топлив. На практике часть выделившейся энергии расходуется на диссоциацию продуктов, поэтому адиабатическая температура горения без учёта диссоциации оказывается заметно выше той, что наблюдается на практике .
Термодинамический расчёт позволяет определить равновесный состав и температуру продуктов, но не даёт никакой информации о том, с какой скоростью система приближается к равновесному состоянию. Полное описание горения требует знания механизма и кинетики реакций и условий тепло- и массообмена с окружающей средой.
4. Типы пламени и скорость горения. Теории горения: тепловая, цепная, диффузионная.
В общем случае скорость горения зависит от скорости смешения исходных компонентов в зоне прогрева и зоне реакции (для гетерогенных систем), от скорости химических реакций между компонентами, от скорости передачи тепла и активных частиц из зоны реакции к исходной системе. Нормальная скорость горения (и тем более форма фронта горения) зависит от условий течения свежей смеси и продуктов горения (особенно при горении в двигателях).
Поэтому в теории горения рассматривается несколько основных типов пламен. Они неодинаковы по своему научному и практическому значению и степени изученности. Неодинаковы параметры, представляющие наибольший интерес для данного типа пламени. Существенно отличается подход к теоретическому рассмотрению каждого типа пламени. Некоторые различия имеются и в экспериментальных методах.
Перечислим наиболее важные для теории горения типы пламен:
1) ламинарное пламя в гомогенной газовой смеси. К этому же типу относится пламя при горении летучих взрывчатых веществ;
2) ламинарное диффузионное пламя при горении струи горючего газа в окислительной атмосфере. К этому типу примыкает пламя при диффузионном горении жидкого горючего, налитого в цилиндрический сосуд, и т. п.;
3) пламя при горении капли жидкого горючего или частицы твердого горючего в окислительной атмосфере;
4) турбулентные пламена в гомогенных или в предварительно не смешанных газовых смесях;
5) пламя при горении нелетучих взрывчатых веществ, порохов и т. д. в тех случаях, когда существенную роль играет реакция в конденсированной фазе.
Коротко рассмотрим некоторые характеристики основных типов пламен в той мере, в какой это полезно для понимания закономерностей горения конденсированных смесей.
Предварительно следует остановиться на определении скорости горения . При ламинарном горении газовых смесей и гомогенных конденсированных систем большое принципиальное значение имеет понятие нормальной скорости горения (uн ). По определейию, uн равна скорости перемещения пламени относительно свежей смеси в направлении, перпендикулярном поверхности пламени в данной точке. Размерность uн в системе СИ - м/сек, однако для скорости горения эта единица пока употребляется редко и только для газовых систем. Обычно величину uн для газовых систем выражают в см/сек, а для конденсированных систем в мм/сек (если выражать скорость горения конденсированных систем в м/сек, то в обычном диапазоне давлений получаются очень малые дробные числа).
Для гомогенных конденсированных систем чаще всего измеряется скорость горения цилиндрических зарядов, горящих с торца, причем фронт горения полагается плоским (опыт показывает, что в большинстве случаев при наличии надлежащей оболочки это допущение справедливо, и искажения наблюдаются лишь на краях заряда). К тому же для твердых веществ (и достаточно вязких жидких веществ) исходное (твердое или жидкое) вещество неподвижно во время горения. Поэтому в данном случае нормальная скорость горения просто равна видимой скорости пламени (в лабораторной системе координат) и постоянна в различных точках заряда.
П. о. веществ и материалов - совокупность свойств веществ (материалов), способствующих возникновению и (или) развитию горения и последующего распространения опасных факторов пожара. П. о. может быть присуща негорючим веществам, которые способны при взаимодействии с др. веществами вызывать горение или усиливать его (функция окислителя); производить тепловую энергию (функция источника зажигания) или горючие газы (функция поставщика горючего). Такие вещества относят к категории особо пожаровзрывоопасных исходя из их несовместимости. Сущность горения заключается в следующем - нагревание источников зажигания горючего материала до начала его теплового разложения. В процессе теплового разложения образуется угарный газ, вода и большое количество тепла. Выделяется также углекислый газ и сажа, которая оседает на окружающем рельефе местности. Время от начала зажигания горючего материала до его воспламенения - называет временем воспламенения. Максимальное время воспламенения - может составлять несколько месяцев. С момента воспламенения начинается пожар
Составляющие пожара и взрыва
Для горения необходимы три элемента:
1. горючее вещество, которое будет испаряться и гореть,
2. кислород для соединения с горючим веществом и
3. теплота для повышения температуры паров горючего вещества до момента их воспламенения.
Символический пожарный треугольник иллюстрирует это положение и дает представление о двух важных факторах, необходимых для предотвращения и тушения пожаров:
1. если одна из сторон треугольника отсутствует, пожар не может начаться;
2. если одну из сторон треугольника исключить, пожар погаснет.
Пожарный треугольник - простейшее представление трех факторов, необходимых для существования пожара, но он не поясняет природу пожара. В частности, он не включает цепную реакцию, возникающую между горючим веществом, кислородом и теплотой в результате химической реакции.
Пожарный тетраэдр - более наглядная иллюстрация процесса сгорания (тетраэдр - это многогранник с четырьмя треугольными гранями). Он очень полезен для понимания процесса сгорания, так как на нем имеется место для цепной реакции и каждая грань касается трех других.
Для осуществления горения необходимы три элемента: горючее вещество (1), кислород (2) и теплота (3), а для поддержания горения - цепная реакция (4).
Процесс горения характеризуется так называемым "пожарным тетраэдром". Если убрать одну из граней тетраэдра, горение прекратится.
Основная разница между пожарным треугольником и пожарным тетраэдром заключается в том, что тетраэдр показывает, каким образом за счет цепной реакции поддерживается пламенное горение, т.е. как грань цепной реакции удерживает остальные три грани от падения.
Цепная реакция начинается следующим образом: образующаяся при горении паров теплота воспламеняет все большее количество паров, при горении которых снова выделяется все большее количество теплоты, воспламеняющей еще большее количество паров. В результате этого постоянно нарастающего процесса горение усиливается. Пока горючего вещества много, пожар продолжает развиваться, пламя разрастается.
Через некоторое время количество паров, выделяющихся из горючего вещества, достигает максимума и начинает стабилизироваться, в результате чего горение протекает с устойчивой скоростью. Это продолжается до тех пор, пока не израсходуется основная часть горючего вещества. Затем окисляется меньшее количество паров и меньше образуется теплоты. Процесс начинает затухать. Происходит выделение все меньшего количества паров, меньше становится теплоты и огня, пожар постепенно угасает. При сгорании твердых горючих веществ может остаться зола, и еще какое-то время будет продолжаться тление. Жидкие горючие вещества выгорают полностью.
ГОРЮЧИЕ ВЕЩЕСТВА (МАТЕРИАЛЫ) – вещества (материалы), способные к взаимодействию с окислителем (кислородом воздуха) в режиме горения. По горючести вещества (материалы) подразделяют на три группы:
§ негорючие вещества и материалы не способные к самостоятельному горению на воздухе;
§ трудногорючие вещества и материалы – способные гореть на воздухе при воздействии дополнительной энергии источника зажигания, но не способные самостоятельно гореть после его удаления;
§ горючие вещества и материалы – способные самостоятельно гореть после воспламенения илисамовоспламенения самовозгорания.
Горючие вещества (материалы) – понятие условное, так как в режимах, отличных от стандартной методики, негорючие и трудногорючие вещества и материалы нередко становятся горючими.
Среди горючих веществ имеются вещества (материалы) в различных агрегатном состоянии: газы, пары, жидкости, твёрдые вещества (материалы), аэрозоли. Практически все органические химические вещества относятся к горючим веществам. Среди неорганических химических веществ также имеются горючие вещества (водород, аммиак, гидриды, сульфиды, азиды, фосфиды, аммиакаты различных элементов).
Горючие вещества (материалы) характеризуются показателями пожарной опасности. Введением в состав этих веществ (материалов) различных добавок (промоторов, антипиренов, ингибиторов ) можно изменять в ту или иную сторону показатели их пожарной опасности.
Окислитель является второй стороной треугольника горения. Обычно в качестве окислителя при горении выступает кислород воздуха, однако могут быть и другие окислители - окислы азота: N,0^, NO, C1, и т.п.
Критическим показателем для кислорода воздуха как окислителя, является его концентрация в воздушной среде закрытого судового помещения в объемных пределах выше 12-14%. Ниже этой концентрации горение абсолютного большинства горючих веществ не происходит. Однако некоторые горючие вещества способны гореть и при более низких концентрациях кислорода в окружающей газовоздушной среде.
САМОВОСПЛАМЕНЕНИЕ - это быстрое самоускорение экзотермической химической реакции, приводящее к появлению яркого свечения - пламени. Самовоспламенение происходит в результате того, что при окислении материала кислородом воздуха образуется тепла больше, чем успевает отводиться за пределы реагирующей системы. Для жидких и газообразных горючих веществ это возникает при критических параметрах температуры и давления.

1 - период загорания 3 - период горения
2 - развития пожара 4 - период затухания
При рассмотрении процессов горения следует различать следующие его виды: вспышка, возгорание, воспламенение, самовоспламенение, самовозгорание, взрыв.
Вспышка- это быстрое сгорание горючей смеси, не сопровождающееся образованием сжатых газов.
Возгорание- возникновение горения под воздействием источника зажигания.
Воспламенение- возгорание, сопровождающееся появлением пламени.
Возгораемость- способность возгораться (воспламеняться) под воздействием источника зажигания.
Самовозгорание- это явление резкого увеличения скорости экзотермических реакций, приводящее к возникновению горения веществ (материала, смеси) при отсутствии источника зажигания.
Самовоспламенение- это самовозгорание, сопровождающееся появлением пламени.
Взрывомназывается чрезвычайно быстрое химическое (взрывчатое) превращение вещества, сопровождающееся выделением энергии и образованием сжатых газов, способных производить механическую работу.
Необходимо понимать различие между процессами возгорания (воспламенения) и самовозгорания (самовоспламенения). Для того чтобы возникло воспламенение, необходимо внести в горючую систему тепловой импульс, имеющий температуру, превышающую температуру самовоспламенения вещества. Возникновение же горения при температурах ниже температуры самовоспламенения относят к процессу самовозгорания (самовоспламенения).
ТЛЕНИЕ - горение твердых веществ (материалов), характеризующееся отсутствием пламени , сравнительно низкими скоростями распространения пламени по веществу (материалу) и температурами 400-600°C, часто сопровождающееся выделением дыма и др. продуктов неполного сгорания. Указанные признаки свидетельствуют о Т. как неинтенсивно протекающем процессе окисления (горения) из-за недостатка окислителя в зоне горения и (или) активно рассеивающейся из этой зоны теплоты. Т. может быть переходной стадией после прекращения пламенного горения материала или удаления внешнего источника зажигания . Такое Т. называютостаточным .
Ожог – это повреждение ткани тела человека из-за внешнего воздействия. К внешним воздействиям можно отнести несколько факторов. Например, термический ожог. Это ожог, который наступил вследствие воздействия горячих жидкостей или пара, предметов сильно раскаленных.
Электрические ожоги – при таком ожоге поражаются еще и внутренние органы электромагнитным полем.
Химические ожоги - те, которые наступили из-за действия йода, например, некоторых растворов кислот. Вообщем различных разъедающих жидкостей.
Если ожог получен вследствие ультрафиолета или инфракрасного излучения, то это лучевой ожог.
По глубине поражения тканей ожоги делятся на четыре степеней.
Ожог 1 степени характеризуется покраснением и небольшим отеком кожных покровов. Обычно выздоровление в этих случаях наступает на четвертые или пятые сутки.
Ожог 2 степени – появление пузырей на покрасневшей коже, которые могут образоваться не сразу. Ожоговые пузыри наполнены прозрачной желтоватой жидкостью, при их разрыве обнажается ярко-красная болезненная поверхность росткового слоя кожи. Заживление, если к ране присоединилась инфекция, происходит в течение десяти – пятнадцати дней, без образования рубца.
Ожог 3 степени – омертвление кожи с образованием струпа серого или черного цвета.
Четвертая степень – омертвление и даже обугливание не только кожи, но и глубже лежащих тканей – мышц, сухожилий, и даже костей. Омертвевшие ткани частично расплавляются и отторгаются в течение нескольких недель. Заживление протекает очень медленно. На месте глубоких ожогов часто образуются грубые рубцы, которые при ожоге лица, шеи и суставов ведут к обезображиванию. На шее и в области суставов при этом, как правило, образуются рубцовые контрактуры.
Поверхность ожогов
Существует процентное соотношение степени поражения всего тела. Для головы – это девять процентов от всего тела. Для каждой руки – тоже девять процентов, грудь – восемнадцать процентов, каждая нога – по восемнадцать процентов и спина также восемнадцать процентов.
Такое деление на процентное соотношение поврежденных тканей к здоровым, позволяет быстро оценить состояние больного и правильно дать заключение можно ли спасти человека.
Вынести пострадавшего из огня, потушить на нем горящую одежду или сорвать ее, охладить обожженные участки тела холодной водой, снегом или льдом до прекращения острых болей.
Самому пострадавшему, если он в сознании и пытается бежать, нельзя сбивать пламя незащищенными руками, нельзя двигаться в горящей одежде, поскольку горение из-за повышенного притока кислорода только усилится. При возможности тут же надо погрузиться в холодную воду, снег.
Обработка обожженных поверхностей должна производиться чистыми руками, чтобы не занести на раневую поверхность инфекцию. Ожоги первой степени обрабатывают семидесяти градусным спиртом или одеколоном. При ожогах второй степени на обожженную поверхность после обработки ее спиртом или одеколоном надо наложить сухую стерильную повязку. Пузыри при этом вскрывать не следует.
Нельзя отрывать от ожоговой поверхности приставшие остатки одежды, их нужно обрезать НПО границе ожога и наложить повязку поверх них. Рот и нос оказывающего помощь и пострадавшего должны быть закрыты марлей или хотя бы чистым носовым платком либо косынкой для того, чтобы при разговоре или дыхании изо рта и носа обожженные места не попадали болезнетворные бактерии, способные вызвать заражение.
При падении сердечно-сосудистой деятельности (снижение артериального давления, учащение пульса при слабом его наполнении) можно ввести подкожно 1-2 ампулы кофеина, кордиамина. Пострадавшего после этого следует укутать в одеяло, но не перегревать его, затем напоить большим количеством жидкости – чаем, минеральной водой, после чего немедленно транспортировать в больницу. И еще: обожженную поверхность нельзя смазывать никакими мазями или засыпать никакими порошками.
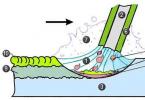
Зона горения (зона активного горения или очаг возгорания) - часть пространства, в котором протекают процессы термического разложения или испарения горючих веществ и материалов (твердых, жидких, газов, паров) в объеме диффузионного факела пламени. Горение может быть пламенным (гомогенным) и беспламенным (гетерогенным). При пламенном горении границами зоны горения являются поверхность горящего материала и тонкий светящийся слой пламени (зона реакции окисления), при беспламенном - раскаленная поверхность горящего вещества. Примером беспламенного горения может служить горение кокса, древесного угля или тление, например, войлока, торфа, хлопка и т.д.
Зона теплового воздействия - это пространство вокруг зоны горения, в котором температура в результате теплообмена достигает значений, вызывающих разрушающее воздействие на окружающие предметы и опасна для человека.
Зона задымления - пространство, смежное с зоной горения, в которое возможно распространение продуктов горения. Скорость выгорания характеризуется потерей массы горючих материалов с единицы поверхности во времени. Этот параметр определяет интенсивность тепловыделения во время пожара, его основные характеристики необходимо учитывать при пожаротушении.
Для прекращения горения необходимо: не допустить проникновения в зону горения окислителя (кислорода воздуха), а также горючего вещества; охладить эту зону ниже температуры воспламенения (самовоспламенения); разбавить горючие вещества негорючими; интенсивно тормозить скорость химических реакций в пламени (ингибированием); механически срывать (отрывать) пламя.
На этих принципиальных методах и основаны известные способы и приемы тушения пожаров.
К огнегасительным веществам относятся: вода, химическая и воздушно-механическая пены, водные растворы солей, инертные и негорючие газы, водяной пар, галоидоуглеводородные огнегасительные составы и сухие огнетушащие порошки.
Вода - наиболее распространенное и доступное средство тушения. Попадая в зону горения, она нагревается и испаряется, поглощая большое количество теплоты, что способствует охлаждению горючих веществ. При ее испарении образуется пар (из 1 л воды - более 1700 л пара), который ограничивает доступ воздуха к очагу горения. Воду применяют для тушения твердых горючих веществ и материалов, тяжелых нефтепродуктов, а также для создания водяных завес и охлаждения объектов, находящихся вблизи очага пожара. Тонкораспыленной водой можно тушить даже легковоспламеняющиеся жидкости. Для тушения плохо смачивающихся веществ (хлопок, торф) в нее вводят вещества, снижающие поверхностное натяжение.
Пена бывает двух видов: химическая и воздушно-механическая.
Химическая пена образуется при взаимодействии щелочного и кислотного растворов в присутствии пенообразователей.
Воздушно - механическая пена представляет собой смесь воздуха (90 %), воды (9,7 %) и пенообразователя (0,3 %). Растекаясь по поверхности горящей жидкости, она блокирует очаг, прекращая доступ кислорода воздуха. Пеной можно тушить и твердые горючие материалы.
Инертные и негорючие газы (диоксид углерода, азот, водяной пар) понижают концентрацию кислорода в очаге горения. Ими можно гасить любые очаги, включая электроустановки. Исключение составляет диоксид углерода, который нельзя применять для тушения щелочных металлов, поскольку при этом происходит реакция его восстановления.
Огнегасительные средства - водные растворы солей. Распространены растворы бикарбоната натрия, хлоридов кальция и аммония, глауберовой соли и др. Соли, выпадая в осадок из водного раствора, образуют изолирующие пленки на поверхности.
Галоидоуглеводородные огнегасительные средства позволяют тормозить реакции горения. К ним относятся: тетрафтордибромметан (хладон 114В2), бромистый метилен, трифторбромметан (хладон 13В1) и др. Эти составы имеют большую плотность, что повышает их эффективность, а низкие температуры замерзания позволяют использовать при низких температурах. Ими можно гасить любые очаги, включая электроустановки, находящиеся под напряжением.
Огнетушащие порошки представляют собой мелкодисперсные минеральные соли с различными добавками, препятствующими их слеживанию и комкованию. Их огнетушащая способность в несколько раз превышает способность галоидоуглеводородов. Они универсальны, так как подавляют горение металлов, которые нельзя тушить водой. В состав порошков входят: бикарбонат натрия, диаммонийфосфат, аммофос, силикагель и т. п.
Все виды пожарной техники подразделяются на следующие группы:
· пожарные машины (автомобили и мотопомпы);
· установки пожаротушения;
· огнетушители;
· средства пожарной сигнализации;
· пожарные спасательные устройства;
· пожарный ручной инструмент;
· пожарный инвентарь.
Горением – называют физико-химический процесс, для которого характерны три признака: химическое превращение, выделение тепла, излучение света
Основа горения – окислительно-восстановительная реакция горючего вещества с окислителем. Окислителями могут быть хлор, бром, сера, кислород, кислородосодержащие и другие вещества.
Однако чаще всего приходится иметь дело с горением в атмосфере воздуха, при этом окислителем является кислород воздушной среды.
Для возникновения горения необходимо наличие:
горючего вещества;
окислителя;
источника воспламенения.
Но и в этом случае горение будет возможным, если горючее вещество и кислород или другой окислитель находятся в определенном количественном соотношении, а тепловой импульс имеет запас тепла, достаточный для нагревания веществ до температуры его воспламенения.
Если мало горючего вещества в смеси с воздухом или мало кислорода (менее 14-16% ), процесс горения не начинается.
Горение может быть вызвано непосредственным воздействием на горючее вещество открытого пламени или накаленного тепла, слабым, но беспрерывным и продолжительным нагреванием горючего вещества, самовозгоранием, химической энергией, механической энергией (трение, удар, давление), лучистой энергией тепла, нагретым до высоких температур воздухом и т.д.
Следовательно, следует различать условия, необходимые для возникновения горения и условия необходимые для протекания процесса горения.
Условия протекания горения:
1. Количество кислорода в составе воздуха, поступающего в зону горения, будет не менее 14–16% , т.е. вещество и окислитель находятся в определенном количественном соотношении.
Температура зоны горения, которая является постоянным источником воспламенения и источником нагрева верхнего слоя горючего вещества, выше температуры его воспламенения.
3. Скорость диффузии горючих газов и паров (продуктов разложения вещества) в зону горения будет несколько выше скорости горения.
4. Количества излучаемого зоной горения тепла при горении вещества будет достаточно для нагрева поверхностного слоя до температуры его воспламенения.
Если одно из этих условий отсутствует, то процесса горения не будет.
Пожарной опасностью называется возможность возникновения или развития пожара, заключенная в каком-либо веществе, состоянии или процессе.
Из этого определения можно сделать вывод, что пожарную опасность представляют вещества и материалы, если они в силу своих свойств, благоприятствуют возникновению или развитию пожара. Такие вещества и материалы относятся к пожароопасным.
Классификация пожароопасных веществ
Пожароопасные вещества по способности к горению подразделяются на:
Трудногорючие;
Негорючие.
Горючими называются вещества, способные самостоятельно гореть после удаления источника зажигания. Горючие вещества в свою очередь разделяются на легковоспламеняющиеся и трудно воспламеняющиеся.
Легковоспламеняющимся веществом называется горючее вещество, способное воспламеняться от кратковременного воздействия пламени спички, искры и тому подобных источников зажигания с низкой энергией.
К ним относятся:
Горючие жидкости (ГЖ):
Анилин ГЖ;
этиленгликоль ГЖ;
моторные и трансформаторные масла ГЖ;
ацетон ЛВЖ;
бензин ЛВЖ;
бензол ЛВЖ;
диэтиловый эфир и др.
ГЖ – жидкость способная самостоятельно гореть после удаления источника зажигания и имеющая температуру вспышки выше 66 0 С .
ЛВЖ – ГЖ, имеющая температуру вспышки не выше 66 0 С.
Горючие газы (ГГ):
пропан и др.
ГГ – газ способный образовывать с воздухом воспламеняемые и взрывоопасные смеси при температурах не выше 55 0 С .
Горючие вещества:
целлулоид;
полистирол;
нафталин;
древесная стружка;
бумага и т.д.
Трудно воспламеняющимися веществами называются горючие вещества, способные воспламеняться только под воздействием мощного источника зажигания.
К ним относятся:
гетинакс;
полихлорвиниловая плитка;
древесина.
Трудно горючими – называют вещества, способные гореть под воздействием источника зажигания, но не способные к самостоятельному горению после удаления его.
К ним относятся:
трихлорацетат натрия (Nа(СН 3 СОО)Сl 3 );
водные растворы спирта;
аммиачная вода и т.д.
Негорючими называют вещества, не способные к горению в атмосфере воздуха обычного состава. К ним относятся: кирпич, бетон, мрамор, и гипс. Среди негорючих веществ имеются много весьма пожароопасных, которые выделяют горючие продукты или тепло при взаимодействии с водой или друг с другом.
К ним относятся:
Карбид кальция (СаС 2 );
Негашеная известь (СаСО 3 );
Разбавленные кислоты с металлами (серная, соляная);
Окислители КМпО 4 , Са 2 О 2 , О 2 , Н 2 О 2 , НО 3 , сжатый и жидкий кислород.
Виды горения — это классификация физико-химического процесса в зависимости от характеристик его протекания.Деление на виды может производиться на основе анализа экзогенных и эндогенных характеристик.
Горение — это стремительно протекающая химическая реакция окисления, сопровождающаяся выделением тепла и свечением. Особенностью этого процесса является наличие цепной реакции распространения огня с ускорением и увеличением количества выделяемого тепла по мере вовлечения в процесс нового материала.
Для обеспечения горения необходимо наличие следующих факторов:
- окислителя (чаще всего это кислород);
- горючего вещества;
- возгорания.
Эти факторы можно разделить на две части: условия и стартовый механизм. К первым относятся:
- состояние среды;
- состояние материала.
Главным фактором среды является наличие такого количества окислителя, который мог бы достаточно долго поддерживать ускоряющуюся цепную реакцию окисления.
Материал должен быть горючим, то есть способным к окислению. К состоянию материала как фактору горения относится и его структура. Пористый материал горит лучше, потому что в нем созданы все условия для лучшего доступа окислителя на всех стадиях процесса.
Стартовый механизм — это возгорание, после которого начинается цепная реакция распространения пламени. Может быть экзогенным и эндогенным. Обычно стремительное окисление начинается от поджога, осуществляемого человеком или природными стихиями.
Человек преднамеренно или нечаянно резко поднимает температуру материала в какой-либо его части, формируя управляемое или неуправляемое (пожар) распространение пламени. Природные стихии — это любой источник высокой температуры. Обычно это вулканы, метеориты, разряды молнии.
Эндогенные причины возгорания — это переход окисления из медленной стадии в быструю. Обычно сам по себе огонь появляется при помещении большого количества горючего материала в среду со значительным содержанием окислителя. Ярким примером является самовозгорание угля или торфа, извлеченных из бескислородной среды на воздух.
Существует еще теория самовозгорания органики при активном действии разлагающих микроорганизмов. Ее суть состоит в том, что бактерии или грибы, разлагая много органики, могут повысить температуру, после чего появляется пламя.
Однако у этой теории есть один изъян: при повышении температуры до определенного предела микроорганизмы перегреваются и прекращают свою деятельность, после чего температура органики снижается. Кроме того, бактерии и грибы могут активно жить только во влажной среде, в которой возникновение пламени невозможно.
Максимальное повышение температуры в разлагающейся куче травы достигает +60°С. После этого бактерии или погибают, или впадают в анабиоз. Через какое-то время на смену перегревшимся микроорганизмам придут другие, но уже в остывшем субстрате.
Виды горения по скорости
Горение — это по определению высокая скорость распространения реакции окисления. Однако есть показатели и побольше. С этой точки зрения виды горения делятся на следующие:
- дефлаграционное — скорость около 10 м/с;
- взрывное — около100 м/с;
- детонационное — около 5000 м/с.
Дефлаграционное горение — это процесс, сопровождаемый передвижением пламени по всему материалу.
Взрыв — это процесс одновременного стремительного окисления всего горючего материала сразу. Обычно он происходит при возгорании очень мелкого и сильно горючего материала.
Детонация — это процесс, при котором распространяется ударная волна, инициирующая реакцию окисления. Последняя поддерживает движение первой за счет стремительно выделяющегося тепла. Ударная волна и экзотермические реакции развивают сверхзвуковую скорость, формируя детонацию.
Эту классификацию не стоит путать с видами пожаров. Понятие последнего произошло не совсем от физики и химии. Это оценка степени управляемости процесса. Горение дров в печке поддается контролю, поэтому это не пожар. В отличие от горения травы и деревьев в лесу.
Разновидности по признакам горючего материала
Конечной стадией горения является сгорание. Оно делится на полное и неполное. Первое — это образование продуктов, которые не являются больше горючим материалом. Обычно это вода, газообразные окислы и минерализованные твердые частицы (зола, пепел). Неполное сгорание происходит в условиях, препятствующих распространению огня. При этом образуются обугленные частички горючего материала.
Внешние условия и виды горения находятся в причинно-следственной взаимосвязи. Примером этого утверждения является деление видов по состоянию смесей.
- Бедные горючие смеси. Это связь какого-либо материала с окислителем, в которой воспламеняющихся компонентов слишком мало для продолжительного процесса окисления. Иными словами, это такая смесь, в которой окислителя много, а гореть нечему. Возможно и обратное: материал горючий и его много, а окислителя слишком мало.
- Богатые смеси. В них соотношение окислителя и горючего материала способствует возникновению устойчивого окисления с высокой температурой. В этой смеси есть чему гореть долго и с большим жаром. Главное, чтобы на этот процесс хватило окислителя.
В норме в воздухе содержится около 21% кислорода. Процесс горения стремительно меняет пропорции состава воздуха. Горение часто становится невозможным при снижении содержания кислорода до 14-18%. В этих неблагоприятных условиях гореть продолжают только некоторые вещества, например водород, этилен, ацетилен. При уменьшении количества кислорода менее 10% горение невозможно для всех смесей.
Процесс хоть и быстрый, но многофакторный. Это позволяет создавать большое количество таксонов и классификаций. Так что разнообразие видов горения зависит не только от среды и материала, но и от фантазии человека.
Горение. Необходимые и достаточные условия, необходимые для обеспечения горения.
Горением называется сложный физико-химический процесс взаимодействия горючего вещества и окислителя, характеризующийся самоускоряющимся химическим превращением и сопровождающийся выделением большого количества тепла и света. Обычно в качестве окислителя участвует кислород, которого в воздухе 21%. Для обеспечения горения необходимо и достаточно: горючее вещество; окислитель; источник воспламенения определенной мощности, обеспечивающий реакцию между горючим веществом и окислителем. Для обеспечения горения горючее вещество и окислитель должны находится в определенных соотношениях друг с другом. Горение, характеризуемое наличием раздела фаз (например, горение твердого вещества), называется гетерогенным. Горение газообразных смесей называется гомогенным.
Горение может осуществляться в двух режимах: самовоспламенения и распространения фронта пламени. Важнейшая особенность процесса горения – самоускоряющийся характер химического превращения.
58.Пожар. Классификация пожаров в зависимости от веществ, подвергаемых горению. Пожаром называется – неконтролируемый процесс горения, сопровождающийся уничтожением материальных ценностей и создающий опасность для жизни людей. Согласно ГОСТу 12.1.004 пожар осуществляется как неконтролируемое горение вне специального очага, причиняющее материальный ущерб. Классификация пожаров в зависимости от веществ, подверженных горению и рекомендуемые средства пожаротушения при этом приведены в таблице 2.4.
А-горение твердых веществ :А1- Горение твердых, веществ, сопровождаемое тлением (например, древесина, бумага, уголь, текстиль); А2-Горение твердых веществ, не сопровождаемое тлением (каучук, пластмассы); В-горение жидких веществ: В1-Горение жидких веществ, нерастворимых в воде (бензин, нефтепродукты), а также сжижаемых твердых веществ (парафин); В2-Горение жидких веществ, растворимых в воде (спирты, ацетон, глицерин и др.); С-горение газообразных веществ: Бытовой газ, пропан, водород, аммиак и др.; Д-горение металлов и металлосодержащих веществ: Д1-Горение легких металлов и их сплавов (алюминий, магний и др.) кроме щелочных; Д2-Горение щелочных металлов (натрий, калий и др.); Д3-Горение металлосодержащих соединений (металлоорганические соединения, гидраты металлов); Класс пожара Е – объект тушения (электроустановки), находящиеся под напряжением. Тушение производится газовыми составами и порошками.